CiPSC平台
Yamanaka四因子方法制备iPSC相较胚胎干细胞方法解决了伦理限制,提高了安全性,体系复杂程度也有所降低,但仍面临着:
慢病毒本身制备周期长,同时转导四个转录因子难度大;
慢病毒自身靠插入宿主细胞基因组表达蛋白,有插入突变风险;
慢病毒制备的iPSC分化的细胞表观基因组不稳定,in vitro和in vivo数据转化差异大等问题。
因此,自2007年开始全世界都在基于四因子方法寻找更好的体内重编程途径。目前主流的方法主要有基于mRNA、仙台病毒、附加型质粒和慢病毒的重编程。 以上四种方法都面临成本高、医用级细胞株建立时间长的问题,而四因子重编程的缺陷本质上来源于对外源生物大分子的依赖。
为了解决这一挑战,北启生物科学创始人邓宏魁博士开发了一种创新技术,使用化学小分子将人类体细胞重编程为人类诱导多能干细胞,这种细胞被称为化学小分子诱导的多能干细胞(CiPSC)。
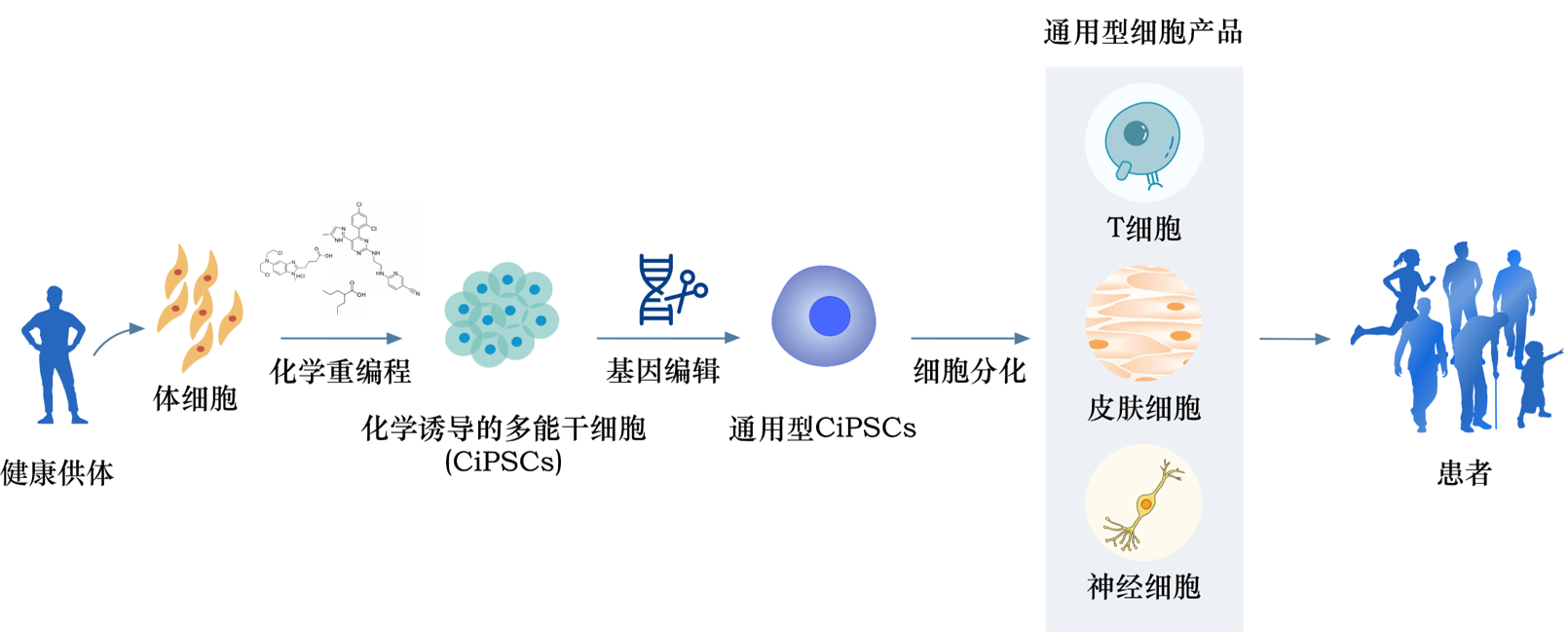
CiPSC技术的主要优势:
安全: 突变率低,重编程因子容易去除,不用担心基因组整合
简单: 透过细胞膜直接作用于靶点,操作方便,可标准化
高效: 细胞重编程效率可达10%以上
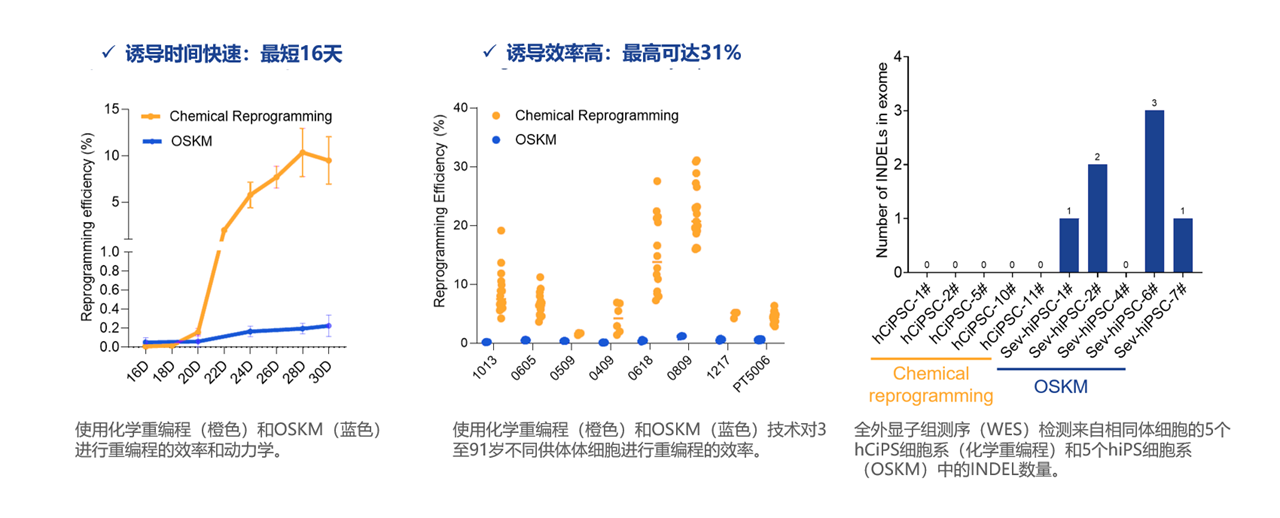
2013,Science,邓宏魁研究团队发表全球第一篇仅使用化学小分子逆转“发育时钟”,让小鼠体细胞重新获得多潜能性的研究。该研究开创了全新的体细胞重编程体系。
Hou et al., Science, 2013
2015,Cell,邓宏魁研究团队发现化学重编程过程中的一个类似于胚外内胚层细胞的中间态 (XEN)-like state,并据此建立了一套更高效的利用小分子化合物诱导化学多潜能干细胞的方案,揭示了化学重编程不同于传统重编程的分子机制。
Zhao et al., Cell, 2015
2018,Cell Stem Cell,邓宏魁研究团队首次在单细胞和全转录组水平系统深入研究了小分子化合物诱导体细胞重编程过程,发现了其中关键分子事件,回答了多能性调控网络是如何逐步建立等重要科学问题,并利用这些启示进一步优化小分子诱导方法,显著加快了重编程进程。
Zhao et al., Cell stem cell, 2018
2022年4月13日,Nature,邓宏魁研究团队首次在国际上报道了使用化学小分子诱导人成体细胞转变为多潜能干细胞这一突破性研究成果。运用化学小分子重编程细胞命运(化学重编程)是继“细胞核移植”和“转录因子诱导”之后新一代的,由我国自主研发的人多潜能干细胞制备技术,为我国干细胞和再生医学的发展解决了底层技术上的瓶颈问题。
Guan et al., Nature, 2022
2022年,Nature medicine,邓宏魁研究团队利用人化学诱导多能干细胞生成了胰岛(hCiPSC-islets),结果表明,将hCiPSC-islets单剂量输注到糖尿病非人灵长类动物体内,可有效恢复内源性胰岛素分泌,改善血糖控制。
Du et al., Nature medicine, 2022
2023年3月20日,北京大学邓宏魁团队在国际学术期刊Cell Stem Cell发表了题为“Highly efficient and rapid generation of human pluripotent stem cells by chemical reprogramming”的研究论文。该研究建立了新的化学重编程体系,更加快速和高效地将人成体细胞诱导为多潜能干细胞,将CiPSC的诱导技术提高到了前所未有的高度。
Shijia et al., Cell stem cell, 2023
2023年5月20日,北启生物联合北京大学第三医院开展“化学小分子重编程建立诱导多能干细胞技术培训班”,培训班由朱家亮博士、刘蓓博士主持,首次在全球范围内公开了北启生物独家开发的试剂盒信息并宣布开放对外销售。
2023年,Nature metabolism,邓宏魁研究团队在这项proof-of-principle研究中发现 hPSC生成的胰岛在移植后存活并逐渐成熟,从而改善了糖尿病灵长类动物的血糖控制。
Liang et al., Nature metabolism, 2023
通用型策略
通用型细胞疗法,是指从健康捐赠者体内提取或利用外周血、脐带血、多能干细胞等途径获取免疫细胞,经过工程改造和扩增最后输入患者体内的疗法,也被称为同种异体(Allogeneic)或现货型("off-the-shelf")免疫细胞疗法。
相较于传统的个体化疗法,通用型细胞疗法主要具有以下四大优点:
 方便进行重复给药
方便进行重复给药
 全流程治疗费用较低,减轻患者及其家庭经济负担
全流程治疗费用较低,减轻患者及其家庭经济负担
 无需进行个体化细胞制备,避免细胞制备周期长对于治疗的延误
无需进行个体化细胞制备,避免细胞制备周期长对于治疗的延误
 适用于更多疾病阶段的病人,如已经过多轮化疗,体内淋巴细胞含量已无法支持重新提取PBMC制备T细胞的患者
适用于更多疾病阶段的病人,如已经过多轮化疗,体内淋巴细胞含量已无法支持重新提取PBMC制备T细胞的患者
